Die Etablierung von Next-Generation Sequencing (NGS) hat unsere Herangehensweise an wissenschaftliche und diagnostische Fragen grundlegend verändert. Das Potenzial von NGS, große Mengen an Sequenzierdaten zu einem verhältnismäßig niedrigen Preis zu erzeugen, führte zu einer Reihe bahnbrechender Entdeckungen und leitete eine neue Ära der Genomik ein. Mit der Entwicklung weiterer Technologien wie Single-Molecule-Real-Time (SMRT) Sequencing im Rahmen des sogenannten Third-Generation Sequencing (TGS) steht nun auch der Aufklärung großer struktureller Varianten nichts mehr im Wege.
Für Ready to Load Sequencing im Hochdurchsatzverfahren stehen Ihnen bei uns fünf Illumina NovaSeq™ 6000 und vier NovaSeq™ X Plus Sequenziersysteme zur Verfügung. Des Weiteren können wir für kleinere Projekte auf zwei MiSeq-Sequencer zurückgreifen. Für TGS und damit für qualitativ hochwertige Long-Read-Sequenzierung sind die PacBio-Plattformen Revio und Sequel® IIe etabliert. Gesammelt können wir so ein breites Spektrum an Optionen für Forschungsprojekte und Pharmastudien anbieten.
Seit ihrer Gründung hat sich die CeGaT GmbH auf den Einsatz von NGS spezialisiert. Wir investieren kontinuierlich in die neusten Technologien, um für unsere Kundinnen und Kunden präzise und zuverlässige Ergebnisse zu erzielen. Unser fundiertes diagnostisches Wissen und unsere bioinformatische Expertise werden durch hochmoderne Laborprozesse und Sequenzierungstechnologien ergänzt. Wir bieten Ihnen eine einzigartige Kombination aus Know-how, den neuesten Technologien und erstklassigem Service für Ihre Projekte.
Unser Team verfügt über umfangreiche Erfahrung mit menschlichen und tierischen Proben sowie über fundierte Expertise in der Bearbeitung von pflanzlichen, mikrobiellen und Pilzproben.
Dank des langjährigen Einsatzes von NGS-Technologien können wir nach der Bearbeitung tausender Proben auf unsere Erfahrung mit Hochdurchsatztechnologien setzen. Unsere Labore sind mit Liquid-Handling-Plattformen von Hamilton ausgestattet. Diese Plattformen lassen sich individuell programmieren, sodass wir unsere Abläufe gezielt an Ihre Anforderungen anpassen können.
Durch den in unseren Laboren etablierten Einsatz von Multiplex-Strategien ermöglichen wir die gleichzeitige Sequenzierung von Hunderten von Proben in einem Sequenzierlauf oder sogar auf einzelnen Flow-Cell-Lanes.
Gerne demonstrieren wir Ihnen die Umsetzbarkeit Ihrer Hochdurchsatzprojekte in einer Pilotstudie.
Illumina-Sequenzierplattformen
Illumina NovaSeq™ X Plus System
- Für Sequenzierung mit hohem Durchsatz und außergewöhnlicher Genauigkeit
- Ideal für die Durchführung größerer Studien und datenintensiver Projekte
- Erzeugt pro Lauf mit zwei Flow Cells bis zu 16 Tb Daten in 48 Stunden
Finden Sie hier einen Performance-Vergleich unserer NovaSeq™ Geräte.

Verwendet unter Lizenz von Illumina, Inc. Alle Rechte vorbehalten.
Illumina NovaSeq™ 6000 System
- Für Short-Read-Sequenzierung mit hohem Durchsatz und niedrigsten Kosten pro Base
- Ideal für Großprojekte und Projekte mit Tiefensequenzierung
- Erzeugt bis zu 6 Tb Daten in 20 Stunden
Finden Sie hier einen Performance-Vergleich unserer NovaSeq™ Geräte.

Verwendet unter Lizenz von Illumina, Inc. Alle Rechte vorbehalten.
Illumina MiSeq™ System
- Für kleine Sequenzierprojekte mit mehreren Konfigurationen
- Readlänge bis zu 2 x 300 bp

Verwendet unter Lizenz von Illumina, Inc. Alle Rechte vorbehalten.
Illumina Workflow
Vorbereitung der Sequenzier-Library
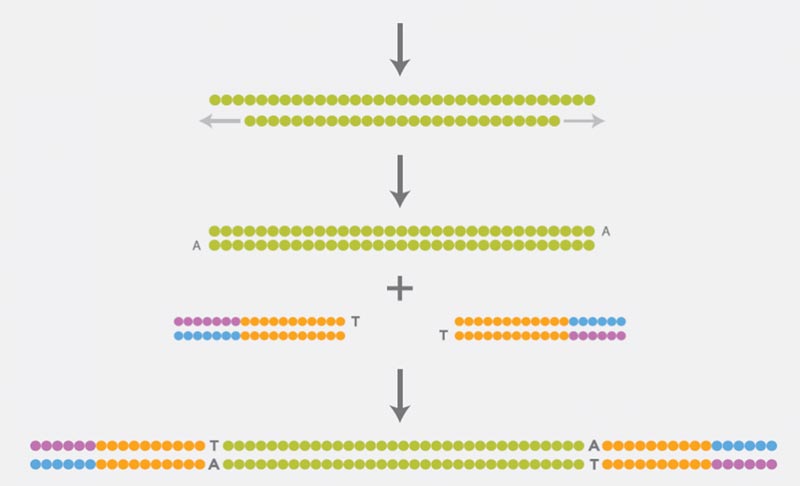
Zunächst wird die DNA fragmentiert, anschließend werden die durch die Fragmentierung beschädigten DNA-Enden repariert. An die freien Enden werden Adapter ligiert; diese enthalten Sequenzmotive, welche für alle nachfolgenden Schritte (klonale Amplifikation und Sequenzierung) benötigt werden. Mit diesem Schritt ist die Vorbereitung der Library abgeschlossen und sie kann auf die Flow Cell geladen werden.
Klonale Amplifikation
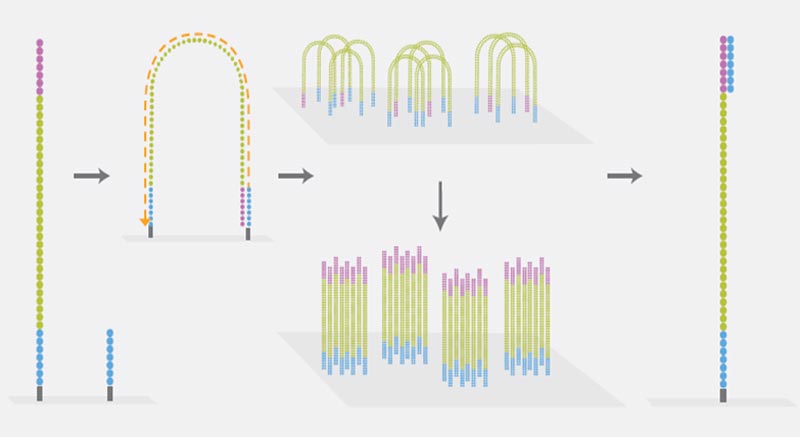
Zur klonalen Amplifikation der einzelnen DNA-Fragmente nutzt die Illumina-Sequenziertechnologie die sogenannte Brücken-PCR („bridge PCR“). Über die zuvor ligierten Adapter binden die DNA-Fragmente an die Flow Cell. Dort werden separate Cluster identischer DNA-Fragmente generiert.
Sequenzierung
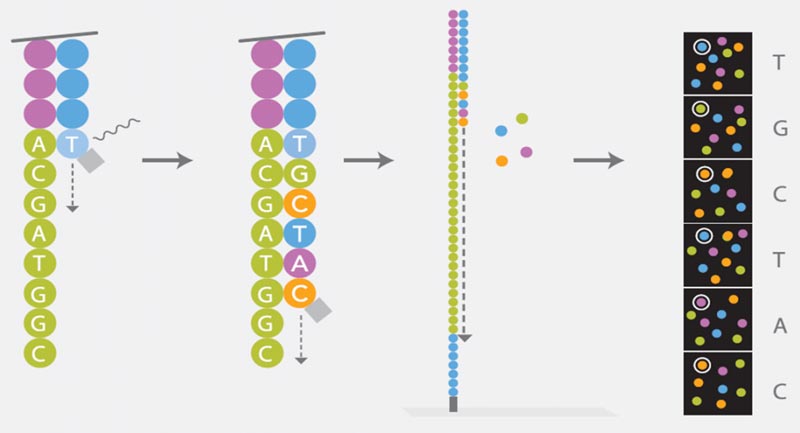
Die Sequenzierung-durch-Synthese-Methode („Sequencing by Synthesis“, SBS) von Illumina basiert auf dem Prinzip der sogenannten zyklisch-reversible Termination („Cycle Reversible Termination“, CRT). Jedes der vier Nukleotide ist mit einem anderen Farbstoff gekoppelt und durch eine Terminatorgruppe modifiziert. Die Polymerase amplifiziert komplementäre Stränge zu den Einzelsträngen im Cluster; dabei werden immer alle vier markierten Nukleotide gleichzeitig angeboten. Nach dem Einbau eines komplementären Nukleotids ist eine Verlängerung aufgrund der blockierenden Wirkung der Terminatorgruppe nicht mehr möglich. Die jeweilige Farbe des eingebauten Nukleotids kann mit Hilfe bildgebender Verfahren nachgewiesen werden. Der Farbstoff und die Terminatorgruppe werden abgespalten und ein neuer Synthesezyklus beginnt. Die Sequenz eines jeden Clusters wird somit gleichzeitig Base für Base bestimmt und erfasst.
PacBio Sequenzierplattformen
PacBio Revio System
- Für HiFi-Sequenzierung von Long-Reads in hoher Qualität
- Beim Einsatz von vier SMRT Cells wird ein Output von bis zu 480 Gb pro Lauf erreicht -mit einer Genauigkeit von 99,95%
- Direkte Bestimmung von Methylierungsmustern mit Hilfe der erfassten Kinetik

Bild zur Verfügung gestellt von PacBio
PacBio Sequel® IIe System
- Für HiFi-Sequenzierung von Long-Reads in hoher Qualität
- Pro Lauf können bis zu 25 Gb an Output erreicht werden – mit einer Genauigkeit von 99,9%
PacBio Workflow
Vorbereitung der Sequenzier-Library
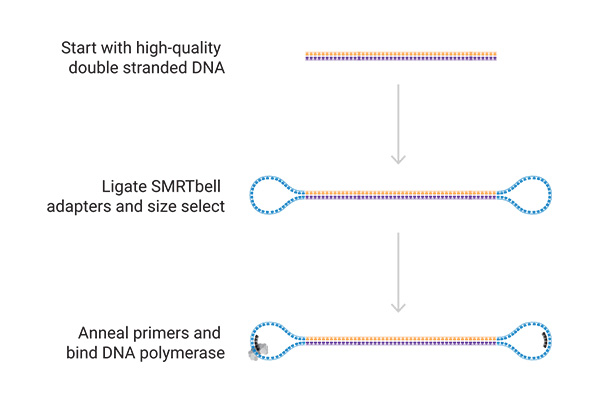
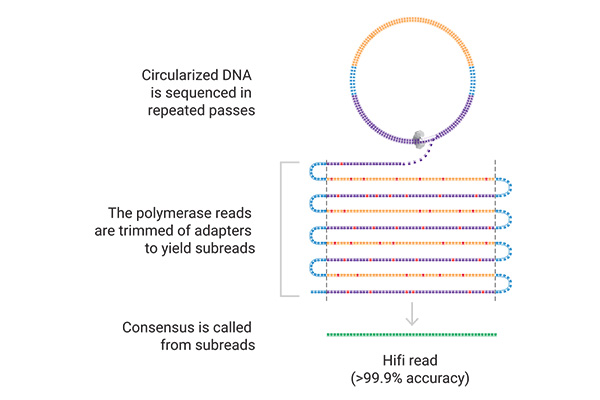
Hairpin-Sequenzieradapter werden an hochmolekulare, doppelsträngige DNA ligiert, wodurch ringförmige DNA-Moleküle, sogenannte SMRTbells®, entstehen. Anschließend werden die Sequenzierprimer und die Polymerase an die Adaptersequenz gebunden. Die fertige Library kann nun auf die SMRT®-Cell geladen werden.
Sequenzierung
Die SMRT®-Cell enthält Millionen von Vertiefungen, sogenannte „Zero-Mode-Waveguides“ (ZMWs). Beim Beladen werden einzelne DNA-Moleküle in diesen Vertiefungen gebunden, und die DNA-Polymerase beginnt, die zirkuläre DNA in Runden zu amplifizieren. Die hierbei eingebauten Nukleotide sind fluoreszenzmarkiert und emittieren beim Einbau in den DNA-Strang Licht. Durch die Erfassung des Lichts beim Nukleotideinbau ist es möglich, die DNA-Sequenz Base für Base in Echtzeit zu verfolgen. Durch mehrfache Amplifikationsdurchläufe desselben DNA-Moleküls und das spätere Zusammenführen dieser Daten werden hierbei hochpräzise Long-Reads (sogenannte HiFi-Reads) erzeugt.
10x Genomics®-Plattform
Unsere 10x Genomics® Plattformen dienen nicht der DNA-Sequenzierung selbst (diese findet auf unseren anderen Plattformen statt), sondern der Vorbereitung von Proben für Sequenzierung auf Einzelzell-Ebene.
10x Genomics® Chromium™ X Controller
- Für die Analyse einzelner Zellen im großen Maßstab
- Mikrofluidik-System zur Erfassung zehntausender einzelner Zellen pro Probe

Bild zur Verfügung gestellt von 10x Genomics, Inc.
Der 10x Genomics® Chromium Workflow
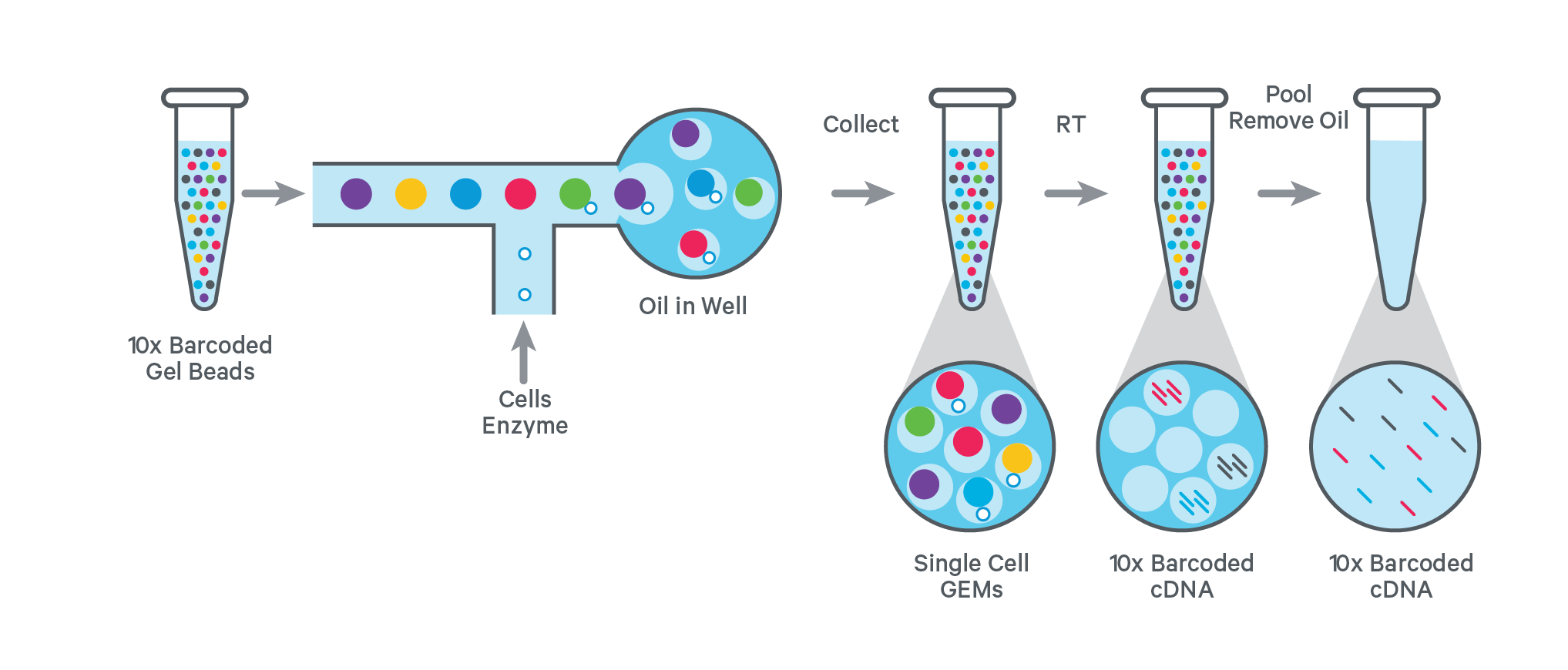
Erzeugung von Gel Beads in Emulsion
Auf dem Chromium-Chip werden sogenannte Gel Beads in Emulsion (GEMs) erzeugt: Hierbei werden 10x barcodierte Gel Beads mit einem MasterMix, welcher die Zellen enthält, und einem Trennöl kombiniert, was zur Bildung von Tröpfchen führt, welche einen 10x barcodierten Gel Bead und eine Zelle enthalten (Einzelzell-GEMs).
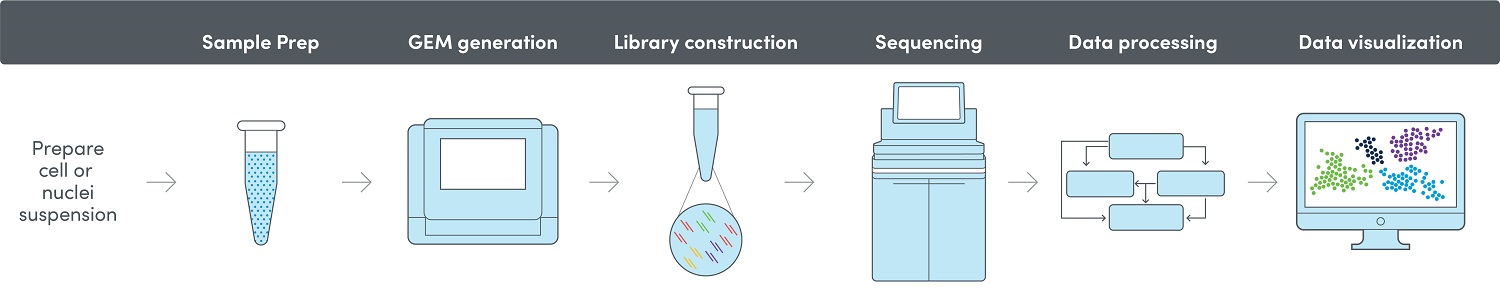
Vorbereitung der Library und Sequenzierung
Nach der GEM-Herstellung lösen sich die Gelkügelchen auf und geben Oligos und Enzyme in die Lösung ab. Bei der darauffolgenden Amplifikation entstehen 10x barcodierte cDNA Fragmente in jedem Tröpfchen.
Anschließend werden alle barcodierten Fragmente der einzelnen GEMs gepoolt und für die Sequenzierung vorbereitet. Die Sequenzierung der Libraries erfolgt auf einer unserer Illumina Plattformen.
10x Genomics® Visium Workflow
Vorbereitung des Gewebes
Ultradünne FFPE-Gewebeschnitte werden auf Glas-Objektträger übertragen. Um die histologische Struktur festzuhalten, werden die Schnitte anschließend mit H&E gefärbt und fotografiert.
Transfer von Sonden mit dem Visium CytAssist
Für die Analyse der Genexpression wird ein Mix unterschiedlicher Sonden auf den Objektträger aufgebracht; diese binden an die RNA im Gewebe. Für die spätere räumliche Zuordnung wird nun ein Hellfeldbild aufgenommen. Anschließend werden alle Sonden, die an RNA gebunden haben, in den Erfassungsbereich eines Visium-Objekträgers übertragen. Diese übertragenen Sonden werden durch positionsspezifische Barcodes verlängert und anschließend vom Visium-Objektträger abgelöst.
Vorbereitung der Library und Sequenzierung
Die barcodierten Sonden werden in einem gemeinsamen Ansatz für die Sequenzierung auf einer der Illumina-Plattformen vorbereitet und anschließend sequenziert. Abschließend wird die Information zur Genexpression mit dem histologischen Bild überlagert, wodurch eine Genexpressionskarte entsteht.
Kontaktieren Sie uns
Sie haben noch Fragen oder Interesse an unserem Service? Treten Sie gern mit uns in Kontakt. Wir werden uns schnellstmöglich um Ihr Anliegen kümmern.
Starten Sie Ihr Projekt mit uns
Gerne beraten wir Sie zu unseren Sequenzierdienstleitungen und erarbeiten mit Ihnen gemeinsam die beste Lösung, die auf Ihre klinische Studie oder Forschungsprojekt abgestimmt ist.
Bitte geben Sie, falls möglich, folgende Probeninformationen an: Ausgangsmaterial, Anzahl der Proben, bevorzugte Option für die Vorbereitung der Library, bevorzugte Sequenziertiefe und gewünschte bioinformatische Analysestufe.